منیزیم، از استخراج و تولید تا مصرف
فلز منیزیم هشتمین عنصر فراوان در طبیعت می باشد و 2.4 درصد از پوسته زمین از این عنصر تشکیل شده است. به دلیل واکنش پذیری قوی آن، بصورت خالص در طبیعت یافت نمی شود و عمدتاً آن را بصورت مجموعه گسترده ای از ترکیبات شیمیایی در آب دریا، صخره و شورابه ها پیدا می کنند.
کانه ها و مواد خام
در بین مشتقات منیزیم، فراوان ترین آن ها دولومیت (ترکیبی از منیزیم و کلسیم کربنات) و منیزیت (منیزیم کربنات) می باشد. ترکیباتی با فراوانی کمتری از جمله ترکیب هیدروکسیدی آن یعنی منیزیم هیدروکسید که به آن بروسیت (Brucite) هم گفته می شود و ترکیب هالیدی آن یعنی کارنالیت (ترکیبی از منیزیم، پتاسیم کلرید و آب) هم وجود دارند.
منیزیم کلرید از شوراب های طبیعی و دریاچه های نمک مانند دریاچه بزرگ نمک واقع در ایالت یوتا، که این دریاچه دارای 1.1 درصد منیزیم بوده و همچنین بحرالمیت ( 3.4 درصد منیزیم) به دست می آید. اما فعلاً اصلی ترین روش بدست آوردن آن اقیانوس ها هستند. با اینکه آب دریا فقط 0.13 درصد منیزیم کلرید در خود دارد اما چون منبعی تمام نشدنی است، صرفه بیشتری نیز دارد.
معدنکاوی، تغلیظ و تولید
هم دولومیت و هم منیزیت با متد های رایج استخراج و تغلیظ می شوند. کارنالیت معمولاً یا به صورت کانی از زمین کنده شده و یا آن را در آب حل کرده و سپس این آب را به سطح زمین می آورند و کارنالیت را از آن جدا می کنند. شوراب های طبیعی حاوی منیزیم از تبخیر تالاب های بزرگ توسط نور خورشید تشکیل می شوند.
استخراج و پایش
منیزیم یک واکنشگر شیمیایی قوی بوده که توانایی ساخت ترکیبات پایداری را دارد. همچنین می تواند هم در حالت مایع و هم در حال گازی، با اکسیژن و کلر واکنش دهد. این به این معنی است که استخراج این فلز از مواد خام آن فرایندی است که انرژی زیاد و فناوری های مخصوصی را می طلبد. تولید تجاری آن به دو شیوه عمده انجام می شود: اولی برقکافت یا الکترولیز کردن و مورد دوم کاهش دمایی منیزیم اکسید از طریق فرایند پیجن (Pidgeon).
روش الکترولیز زمانی 75 درصد از منیزیم دنیا را تولید می کرد. اما در ابتدای قرن 21، ورود چین به عنوان پیشرو در زمینه تولید منیزیم، هزینه پایین کارگر و انرژی به رایج شدن فرایند پیجن کمک کرد. با وجود اینکه فرایند پیجن از برق کافت کردن بازده پایین تری داشت اما چون صرفه اقتصادی بیشتری را دارا بود به سرعت فراگیر شد.
1. برق کافت یا الکترولیز کردن (Electrolysis)
این فرایند شامل دو مرحله است: در ابتدا آماده کردن منیزیم کلرید به عنوان ماده خام و اولیه و در مرحله بعد، تجزیه کردن این ماده به فلز منیزیم و گاز کلر در سلول های الکترولیزی. در طی این فرایند، مواد اولیه سلول، شامل انواع مختلفی از نمک های مذاب مانند منیزیم کلرید بی آب، منیزیم کلرید کم آب و یا کارنالیت بی آب می باشند.
برای اینکه ناخالصی های موجود در کانی های کارنالیت روند فرایند را مختل نکنند، کارنالیت را بصورت مصنوعی و از تبلور کنترل شده محلول های حاوی منیزیم داغ و پتاسیم تولید تهیه کرده و مصرف می نمایند.
منیزیم کلرید کم آب نیز طی فرایند داو (Dow Process) تولید می شود؛ که در آن آب دریا در یک لخته کننده با دولومیت فعال نیمه سوخته مخلوط می شود. مقداری منیزیم هیدروکسید نامحلول در ته تانکر ته نشینی رسوب کرده که از آنجا به شکل دوغاب برداشته شده، سپس تصفیه و در آخر آن را بوسیله واکنش با هیدروکلریک اسید تبدیل به منیزیم کلرید می کنند. سپس منیزیم کلرید حاصل را طی چند فرایند تبخیر، آب زدایی کرده و میزان آب آن را به 25 درصد می رسانند. آب زدایی نهایی هنگام ذوب این ماده انجام می شود.منیزم کلرید بی آب به دو روش متعارف تولید می شود. آب زدایی دریاچه های منیزیم کلرید و کلردار کردن منیزیم اکسید. در مورد دوم، که در بند قبل مختصر در مورد آن توضیح داده شده، دولومیت نیمه سوخته با آب دریا در یک لخته کننده مخلوط می شود. سپس از لخته کننده منیزیم هیدروکسید ته نشین شده، سپس آن را فیلتر و با دمای زیاد خشک می کنند تا تبدیل به منیزیم اکسید شود. منیزیم اکسید حاصل با زغال و حلال منیزیم کلرید مخلوط شده و سپس خشک شده و به دستگاه کلر زن برده می شود. این دستگاه، نوعی اجاق است که بوسیله الکترود های کربنی تا دمای 1000 الی 1200 درجه سانتی گراد داغ می شود. گاز کلر به درون این اجاق هدایت شده و با منیزیم اکسید واکنش داده و منیزیم کلرید مذاب تولید می کند که منیزیم کلرید حاصل در فواصل زمانی معینی به درون سلول های الکترولیز جاری می شود.
سلول های الکترولیز اساساً محفظه هایی هستند که به چندین کاتد از جنس استیل و آند از جنس گرافیت مجهز شده اند. کاتد و آند در سلول به صورت عمودی قرار گرفته و به درون نمک مذاب آلکالین کلرید فرو می روند که در طی آن منیزیم مذابی که در فرایند های بالا تولید شده به این نمک مذاب به نسبت 6 الی 18 درصد اضافه، تجزیه شده و از آن منیزیم خالص و گاز کلر به دست می آید. این فرایند در دمایی بین 680 تا 750 درجه سانتی گراد انجام شده و در طی آن 12 الی 18 کیلووات ساعت توان به ازای هر کیلوگرم منیزیم تولیدی مصرف می شود. کلر و دیگر گاز های تولیدی بر روی آند های گرافیتی تشکیل می شوند، و منیزیم مذاب بر روی نمک مذاب شناور شده که از همانجا برداشت می شود. گاز کلر تولیدی را می توان برای فرایند های آب زدایی بعدی نیز استفاده نمود.
کاهش گرمایی
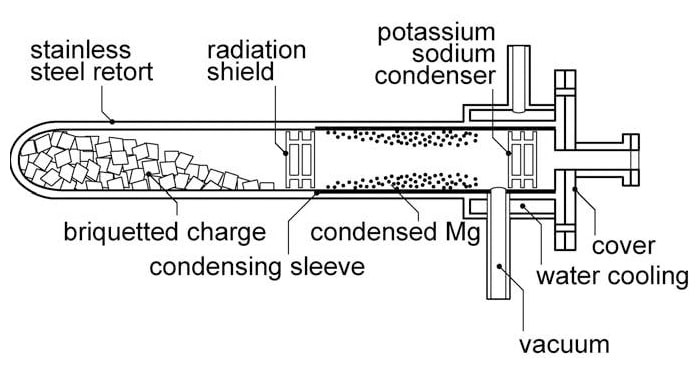
در طی این فرایند دولومیت تکلیس شده (داغ کردن تا دمایی کمتر از نقطه ذوب، در انگلیسی به آن Calcine گفته می شود) و تبدیل به منیزیم اکسید و آهک می شود. این دو نیز سپس به کمک سیلیکون کاهیده شده و در نتیجه از این فرایند، گاز منیزیم و تفاله ای از دی کلسیم سیلیکات به دست می آید. این فرایند گرماگیر است بنابراین باید به آن مقدار کافی گرما داد تا فرایند شروع شده و پایدار بماند. هنگامی که گاز منیزیم به فشار بخار 100 کیلوپاسکال در دمای 1800 درجه سانتی گراد رسید، گرمای مورد نیاز برای ادامه فرایند بیشتر خواهد شد. برای پایین آوردن دمای مورد نیاز واکنش، فرایند های صنعتی در خلاء انجام می شوند. برای تامین گرما نیز سه راه متعارف وجود دارد.
تصفیه سازی
بعد از استخراج منیزیم از فرایند کاهش گرمایی، منیزیم خام به مراکز ریخته گری برای رفع هرگونه ناخالصی، اضافه کردن آلیاژ های لازم و تغییر شکل به شمش، شمش های کوچک و لوح برده می شود.در هنگام ذوب کردن و نگه داری، منیزیم و آلیاژ مذاب بوسیله لایه ای از شار، و یا جریان گازی مانند گوگرد هگزافلوئورید یا گوگرد دی اکسید برای جلوگیری از آتش سوزی محافظت می شوند. برای حمل و نگه داری در شرایط خاص آب و هوایی، به منظور جلوگیری از خوردگی فلز منیزیم را در جعبه های پلاستیکی دارای تهویه و یا ورق های بسته بندی نگه داری می کنند.
By accepting you will be accessing a service provided by a third-party external to https://modirkharid.com/mag/